- Productos
- Oncohematología
- Inmunología
- Anticuerpos
- Reactivos individuales
- Determinación de compatibilidad cruzada (FCXM)
- FcεR1
- Subclases Ig
- Reactivos individuales
- Kits
- Solicitar información
- Recursos y soporte
- Anticuerpos
- Exosomas
- Reactivos accesorios
- Software
- Tienda
- Servicios
- Síntesis de Péptidos
- Diseño
- Modificación
- Servicios de Proteínas
- Expresión y purificación
- Liofilización
- Desarrollo de anticuerpos
- Monoclonal
- Policlonal
- Servicios especializados de anticuerpos
- OEM/Producción a granel
- Purificación
- Conjugación
- Servicios de exosomas
- Aislamiento y purificación
- Caracterización
- Síntesis de Péptidos
- Soporte
- Sobre nosotros
- Contacto
Células CAR T:
Reconocimiento y discriminación de alta resolución con un solo reactivo
Con la creciente importancia de la terapia con células CAR T en el tratamiento del cáncer, es crucial garantizar el éxito de la modificación y monitorización de los linfocitos T modificados.
Nuestro reactivo de citometría de flujo simplifica este proceso, permitiendo a los especialistas confirmar ambos retos clave con un sencillo protocolo de 1 hora.
Experimenta el poder de la precisión y la eficacia reconociendo y discriminando las células CAR T del resto con alta resolución.
REFERENCIAS DE PRODUCTO
| Product name | Reference | Description | |
|---|---|---|---|
CD19 CAR-T | 19-0212-25T | Human PE-CD19 | RUO | 25 test | Ir a la tienda |
CD19 CAR-T | 19-0212-100T | Human PE-CD19 | RUO | 100 test | Ir a la tienda |
CD19 CAR-T | 19-0213-25T | Human FITC-CD19 | RUO | 25 test | Ir a la tienda |
CD19 CAR-T | 19-0213-100T | Human FITC-CD19 | RUO | 100 test | Ir a la tienda |
BCMA CAR-T | BCMA-0312-25T | Human PE-BCMA | RUO | 25 test | Ir a la tienda |
BCMA CAR-T | BCMA-0312-100T | Human PE-BCMA | RUO | 100 test | Ir a la tienda |
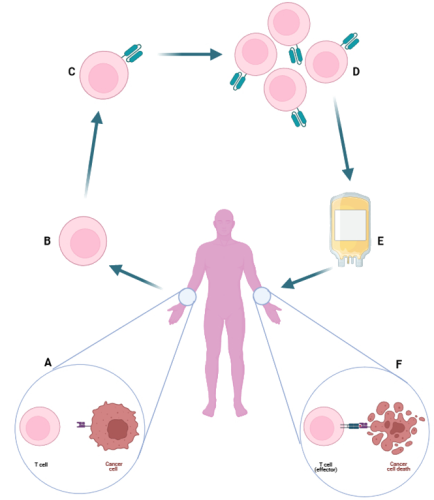
La terapia con células CAR T se basa en la extracción de linfocitos T del paciente, la introducción de un Receptor Antígeno Quimérico (CAR) específico de una proteína presente en las células cancerosas (por ejemplo, CD19, BCMA) y la consiguiente reinfusión de estas células modificadas, ahora llamadas células CAR T, en el paciente para que reconozcan las células diana y las eliminen.
Esta terapia ha cobrado relevancia por su eficacia, por lo que las herramientas de detección de células CAR T se han convertido en una necesidad crítica, tanto para comprobar que han sido modificadas correctamente como para monitorizarlas tras la reinfusión, ya que tienen una vida útil limitada.
Figura 1: Esquema básico de la terapia con células CAR T. (A) La célula T propia no reconoce la célula cancerosa. (B) Extracción de la célula T. (C) Modificación de la célula T con CAR. (D) Cultivo y recolección de células CAR T. (E) Las células CAR T recolectadas se reinfunden en el paciente. (F) La célula CAR T reconoce y elimina la célula cancerosa.
Una solución diferencial
Identifica células CAR T de otras poblaciones con alta resolución, incluso con muestras difíciles

Un único reactivo.
Protocolo simple y rápido (1 hora)
Fluorocromo compatible con
cualquier Citómetro de Flujo (R-PE)

Compatible con paneles de
más de 30 anticuerpos
Limitaciones de los Reactivos Actuales
Existen algunos reactivos para identificar y cuantificar las células CAR T, basados en CD19 o BCMA recombinante marcado con fluorescencia (PE o FITC). Sin embargo, los reactivos actuales presentan limitaciones a la hora de separar con sensibilidad las poblaciones deseadas, lo que dificulta a los analistas la obtención de un resultado preciso y fiable.
Los reactivos que superan este problema tienen la desventaja de implicar protocolos más complejos y lentos, utilizando un reactivo de amplificación además de la proteína. Por lo tanto, es necesario introducir nuevos reactivos simples, sencillos y fáciles de usar que sean capaces de discriminar claramente las células CAR T del resto de poblaciones para obtener un análisis más fiable.
Figura 2: Protocolo FACS (Fluorescent-Activated Cell Sorting). Immunostep frente a competidores. Otros competidores requieren más pasos y reactivos (competidor 1) o protocolos más largos (competidor 2). Immunostep combina la simplicidad con la rapidez, proporcionando a los analistas un protocolo más sencillo.
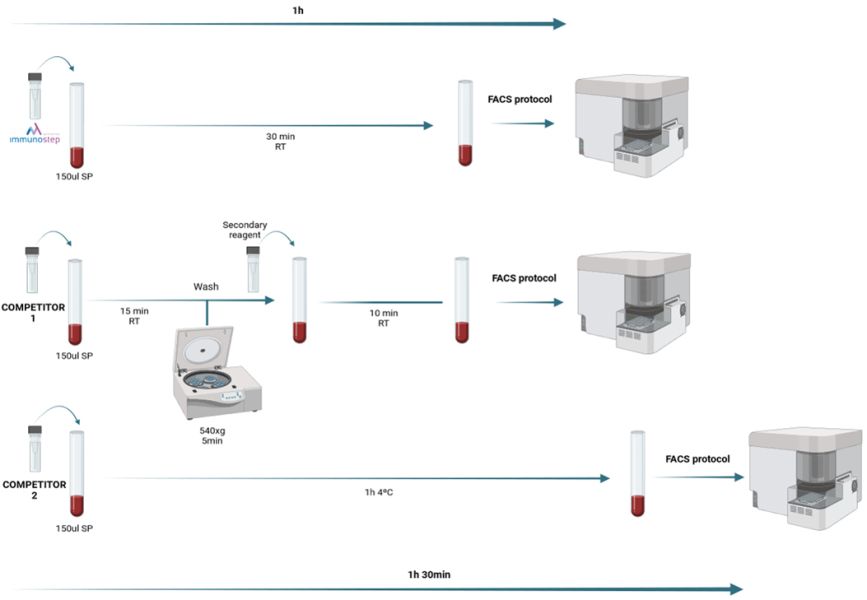
El reactivo se suministra en solución acuosa para el marcaje celular directo con 5 μl del mismo. Esto, con el uso de un panel de anticuerpos para discriminar las células T, es suficiente para separar las que tienen CAR en sólo 30 minutos de incubación a temperatura ambiente (TA), empleando alrededor de 1 hora de protocolo completo, mientras que otros protocolos emplean el mismo tiempo sólo para etiquetar la población específica (ver figura 2).
Otros reactivos comerciales se basan en una tinción indirecta, con una proteína biotinilada que debe ser revelada por un reactivo secundario fluorescente. Esta estrategia tiene buenos resultados, pero un coste elevado y un protocolo más complejo.
Detección de células CAR T
Para satisfacer estas necesidades, hemos desarrollado un reactivo único para el reconocimiento directo y específico de las células CAR T con alta resolución. Este reactivo permite a los especialistas confirmar la modificación exitosa de los linfocitos T en un control de calidad previo a la infusión en el paciente y monitorizarlos después de este paso.
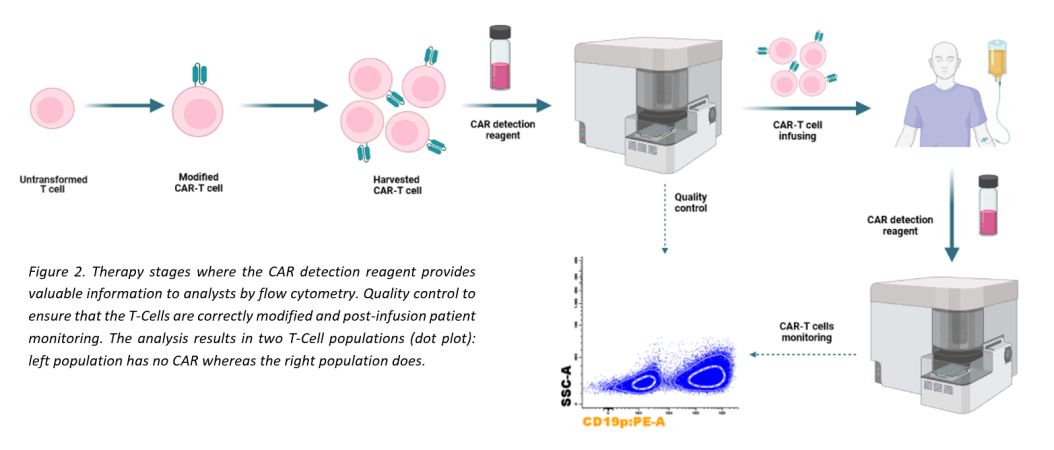
TECNOLOGÍA
La proteína CD19 y BCMA recombinante Fc-Tag (CD19p) ha sido marcada, mediante un proceso propio, con el fluorocromo R-Ficoeritrina (R-PE o PE) o FITC, obteniendo un conjugado que es capaz de ser reconocido por las células CAR T y las separa eficientemente sin ningún reactivo secundario.
Otros fabricantes disponen de productos similares basados en este complejo fluorocromo-proteína pero presentan limitaciones en la separación debido a las técnicas de bioconjugación y/o al fluorocromo utilizado.
BrightStepTM: nuestra tecnología de etiquetado patentada
Esta tecnología de vanguardia está llamada a redefinir la detección de células CAR T. Con BrightStep, hemos mejorado el arte del etiquetado, garantizando el mantenimiento de la conformación y las modificaciones naturales de la proteína. Esto significa una precisión sin precedentes sin necesidad de comprometer la integridad de la muestra.
Verificado mediante rigurosas pruebas de Citometría de Flujo, Brightstep ofrece un mayor rendimiento en especificidad y sensibilidad. Puede confiar en su fiabilidad para obtener resultados precisos en todo momento.
Además, gracias a la consistencia y reproducibilidad entre lotes, puede confiar en BrightStep para garantizar resultados fiables en sus necesidades de investigación y diagnóstico.
Experimenta el futuro de la detección de células CAR T con BrightStep, donde la innovación se une a la precisión.
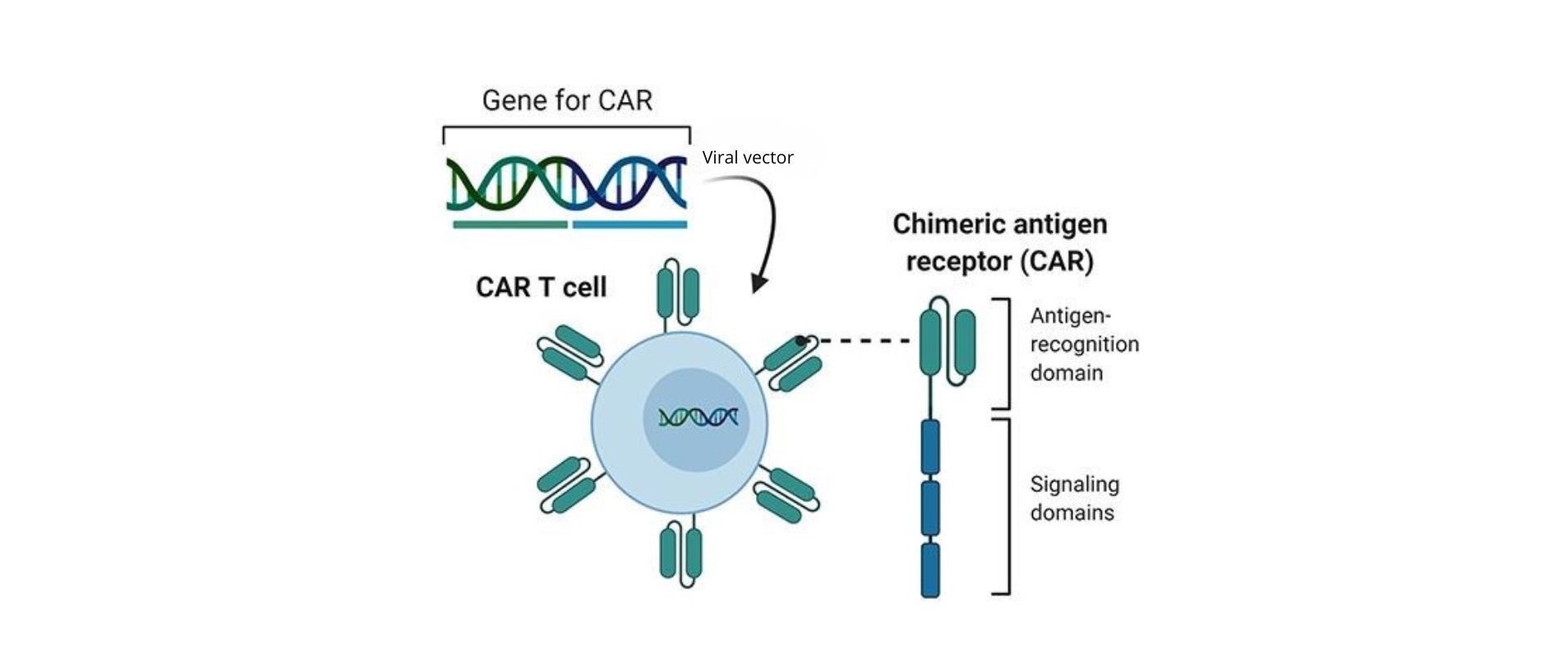
Figura 4: Representación de la modificación de la célula T a célula T CAR y de la estructura del CAR. La célula T se transfecta con un vector viral que contiene la información para expresar el CAR. Éste se compone de un dominio extracelular que reconoce específicamente el antígeno, diseñado a partir de un anticuerpo, y de otros dominios transmembrana e intracelulares con funciones de señalización y coestimulación que aumentan la eficacia del reconocimiento y la activación de la célula T.
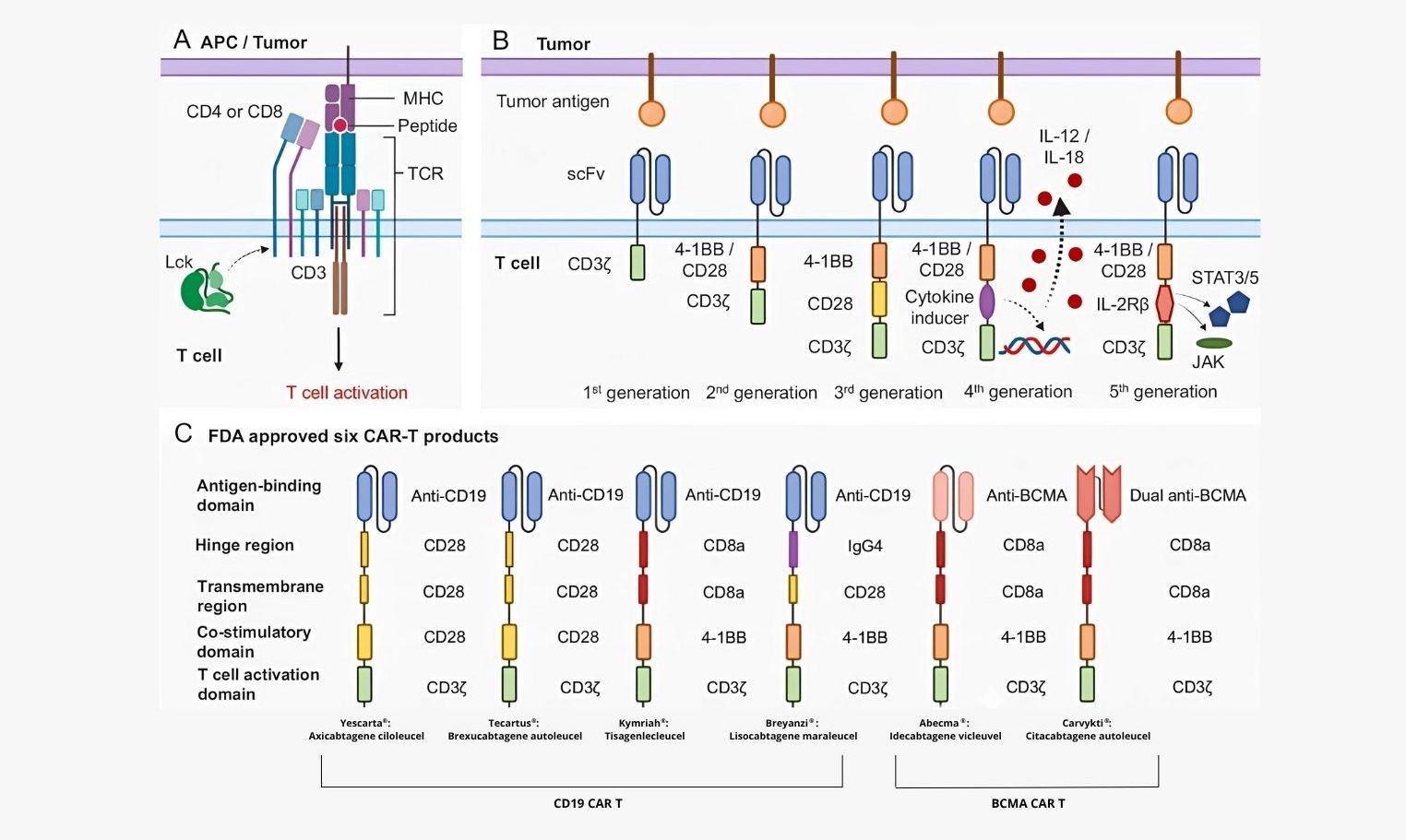
Figura 5: A Cuando una célula T se encuentra con células presentadoras de antígenos o células tumorales, el receptor de células T (TCR) y el complejo CD3, junto con CD4 o CD8, reconocen los péptidos presentados por el complejo MHC y desencadenan la cascada de señalización del TCR, que conduce a la activación de la célula T. B El CAR de primera generación consta principalmente de dos partes: scFv en la parte extracelular y cadena CD3ζ en la parte intracelular. El dominio scFv puede reconocer antígenos de la superficie del tumor y, a continuación, la cadena CD3ζ activará directamente las células T. Los CAR de segunda generación incorporan un dominio de coestimulación, ya sea el dominio de señalización 4-1BB o CD28. El CAR de tercera generación tiene tanto dominios de señalización 4-1BB como CD28. C Diferencias del dominio de unión al antígeno, la región bisagra, la región transmembrana, el dominio coestimulador y el dominio de activación de células T de seis productos CAR-T aprobados por la FDA. Estos productos se utilizan para tratar el linfoma de células B, la leucemia de células B y el mieloma múltiple. APC célula presentadora de antígeno, MHC complejo mayor de histocompatibilidad, TCR receptor de células T, scFv fragmento variable de cadena simple. (Fuente: Nature)
COMPARATIVA ENTRE SOLUCIONES
El fundamento de la citometría de flujo es unir el reactivo a una población específica y discriminarla por la fluorescencia del reactivo. El reactivo se dirige al CAR en la célula T modificada, por lo que la separación depende del nivel de expresión del CAR y de la capacidad discriminatoria del reactivo. El reactivo identifica la población específica por su fluorescencia, pero no es tan importante la intensidad de esa fluorescencia, medida como MFI (Median Fluorescence Intensity), sino la capacidad de discriminar entre la población positiva (CAR T-Cells) y las poblaciones negativas (resto de las células).
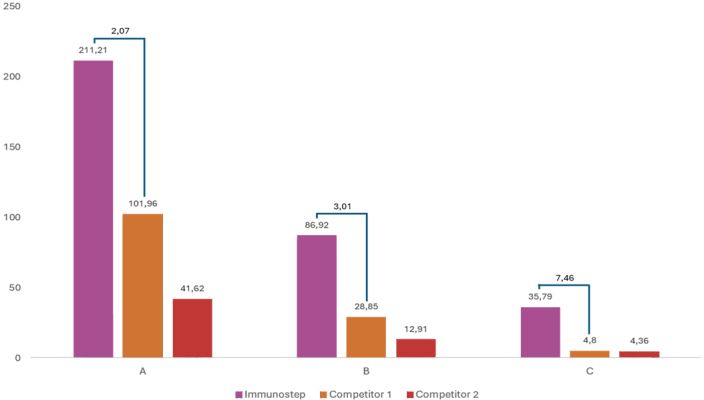
Figure 6: Gráfico de barras que representa la relación entre Immunostep y los otros dos competidores. En la muestra C, la de más difícil discriminación (células CAR T académicas), Immunostep muestra la diferencia más alta, proporcionando un resultado fiable.
Significa que es necesaria la mayor diferencia entre ambas poblaciones MFI; este valor se conoce como Stain Index (SI), a mayor SI mejor discriminación. Un reactivo altamente fluorescente es necesario cuando la cantidad de molécula diana es baja pero a veces también aumenta la MFI negativa, empeorando el SI. Los mejores reactivos tienen un alto SI con una fluorescencia moderada o alta para identificar células CAR T, incluso con baja expresión de CAR.
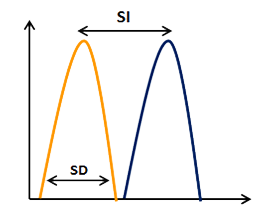
Figura 7: Índice de Tinción, valor para estimar el nivel de discriminación entre poblaciones positivas y negativas.
STAIN INDEX = (Mediana de Positivos – Mediana de Negativos) / (SD de Negativos * 2).
Preguntas Frecuentes (FAQs)
El reactivo PE CD19 CAR Detection tiene una estabilidad de un (1) año en condiciones de refrigeración (4 – 8 ºC). Evitar la congelación y los cambios constantes de temperatura.
Se pueden marcar 100-200 µl de sangre periférica con 5 µl (1 test) de reactivo de detección PE CD19 CAR. Dependiendo de la muestra, puede ser necesario titularla.
La R-Ficoeritrina (R-PE o PE) puede ser excitada a 488 nm (Láser Azul). La mayoría de los Citómetros de Flujo tienen este láser de excitación, por lo que el reactivo de detección PE CD19 CAR puede ser detectado por cualquiera de ellos.
Definitivamente sí. Se ha probado en paneles de hasta 33 reactivos y sigue funcionando. Si el panel tiene muchos reactivos, puede ser necesario titularlo para obtener mejores resultados.